Entwicklung von IVD-Software
Wir begleiten Sie in allen Bereichen
über Web- und Desktop-Anwendungen bis hin zu mobilen Applikationen realisieren wir leistungsfähige, sichere und normenkonforme Software für moderne Diagnostiksysteme.

Leitfaden
IVDR Software: Qualifizierung & Klassifizierung
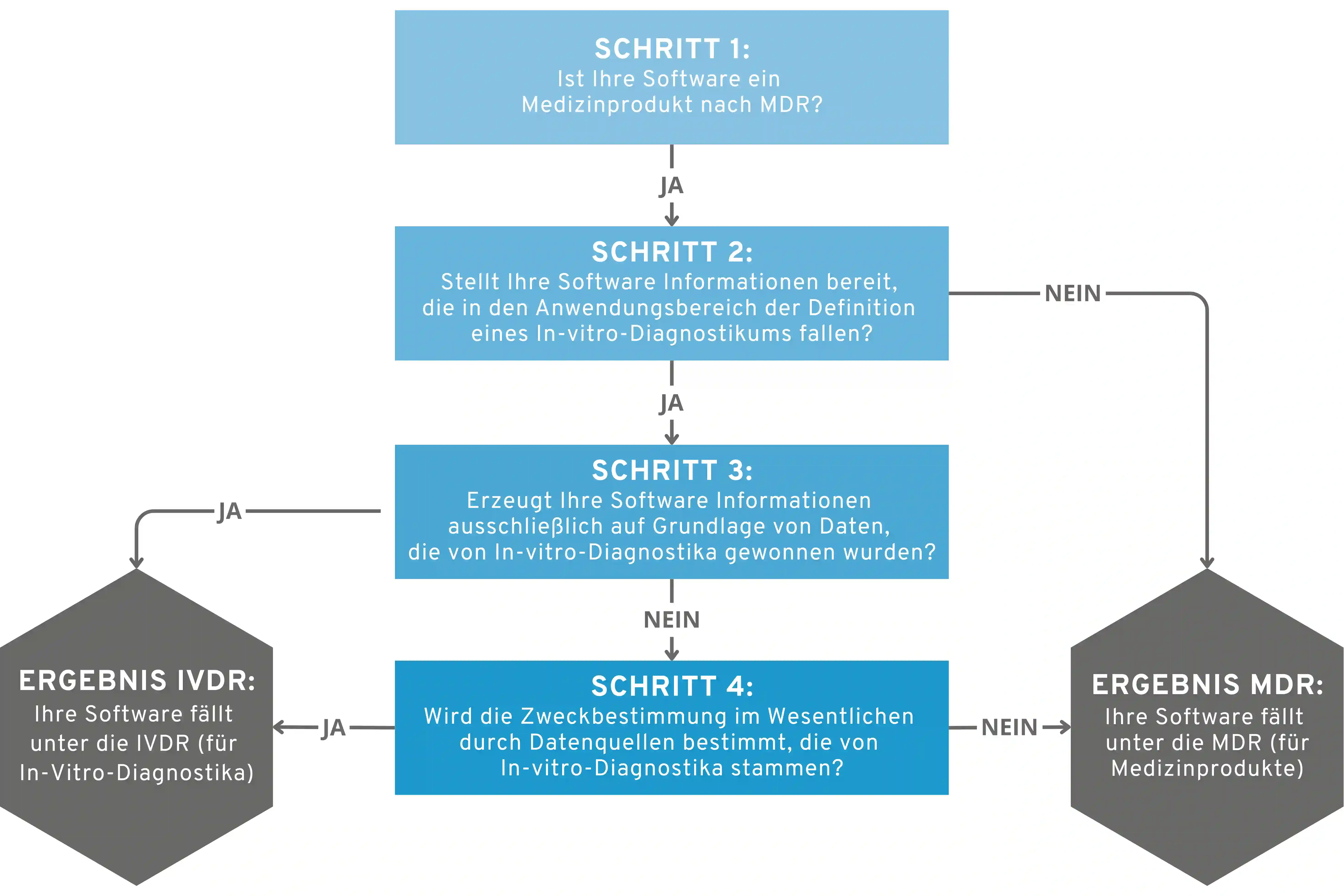
In unserem Leitfaden IVDR Software – Qualifizierung und Klassifizierung erklären wir Ihnen…
- …wann Software unter die In Vitro Diagnostic Regulation (IVDR) fällt
- …wie die Qualifizierung funktioniert
- …und nach welchen Kriterien die Risikoklassifizierung erfolgt.
Unsere Kompetenzen
Software-Entwicklung
- Mobile Apps
- Web-Anwendungen
- Desktop-Anwendungen
- Backend-Komponenten
- Embedded Systeme
Informationssicherheit
-
Zertifizierte Cyber Security nach ISO 27001, IEC 81001-5-1, MDCG 2019-16
-
Penetrationstests nach OWASP & BSI TR-03161
-
Informationssicherheitsmanagement
-
DSGVO-Compliance
Technische Dokumentation nach IVDR
- Qualitätsmanagement (ISO 13485)
- Software-Lebenszyklus-Prozesse (IEC 62304)
- Risikomanagement (ISO 14971)
- Gebrauchstauglichkeit (IEC 62366)
Regulatorische Beratung
- Zulassung als In-vitro-Diagnostikum nach IVDR
- Klassifizierung von In-vitro-Diagnostika
- Identifikation und Umsetzung der IVDR-Anforderungen
- Validierung von IVD-Produkten
Unser Prozess
Wir stehen vom ersten Konzeptentwurf bis zum Betrieb Ihrer IVD-Software an Ihrer Seite. Dabei passen wir unsere Dienstleistungen flexibel an den jeweiligen Stand Ihres Projekts an, um genau die Leistungen bereitzustellen, die Sie benötigen.

1. Konzeption
- Anforderungsanalyse
- Definition der Zweckbestimmung
- Planung der Systemarchitektur
- Auswahl geeigneter Technologien
- Festlegung der regulatorischen Strategie

2. Planung
- Projektplanung
- Definition des Projektteams
- Klärung der Verantwortlichkeiten
- Identifikation von Anforderungen (technisch und regulatorisch)
- Priorisierung von Funktionen
- Risikoanalyse & Planung von Kontrollmaßnahmen (IT- und Patientensicherheit)

3. Entwicklung & Dokumentation
- Technische Umsetzung der Anforderungen
- Agile Entwicklung der IVD-Software
- Einhaltung der IVDR-Anforderungen
- Regulatorische Konformität der Dokumentation
- Produktkennzeichnung

4. Verifizierung & Validierung
- Software-Tests
- Klinische Evaluierung und Prüfung
- Penetrationstests
- Sicherheitsprüfungen

5. Zulassung als In-Vitro-Diagnostikum
- Generierung einer UDI-Nummer
- Anmeldung des Produkts (EUDAMED)
- Begleitung des Audits durch benannte Stellen
-

6. Nach der Zulassung
- Nutzer-Support
- Wartung der IVD-Software
- Nachbeobachtung nach dem Inverkehrbringen
- Klinische Nachbeobachtung
-
IVD-Software-Typen
Wir entwickeln verschiedene Arten von Softwarelösungen für In-vitro-Diagnostika (IVDR), die auf Ihre spezifischen Anforderungen und den Anwendungsbereich abgestimmt sind. Egal, ob Sie eine Standalone-Software, Embedded-Software oder Steuerungssoftware für Geräte benötigen, wir bieten Ihnen maßgeschneiderte Lösungen, die höchste Qualität und Compliance gewährleisten.

Standalone Software
Standalone-Softwarelösungen sind eigenständige Anwendungen, die unabhängig von anderen Systemen arbeiten. Diese Art von Software wird häufig in klinischen Umgebungen verwendet, um Diagnosen zu unterstützen oder Analyseprozesse zu ermöglichen. Wir stellen sicher, dass diese Software nicht nur benutzerfreundlich und zuverlässig ist, sondern auch alle regulatorischen Anforderungen der IVDR erfüllt.

Embedded Software
Für IVDR-Geräte, die mit integrierter Software arbeiten, bieten wir maßgeschneiderte Embedded-Lösungen. Diese Software wird als Teil eines In-vitro-Diagnostik-Geräts integriert und setzt die Kernfunktionalität um. Weitere Informationen zu unseren Embedded-Software-Dienstleistungen finden Sie auf unserer Embedded Software Service-Seite.

Steuerungssoftware für Geräte
Steuerungssoftware ist für die direkte Kontrolle und Bedienung von IVD-Geräten verantwortlich. Sie sorgt dafür, dass das Gerät zuverlässig arbeitet und alle diagnostischen Prozesse ordnungsgemäß ausgeführt werden. Wir gewährleisten die vollständige Einhaltung der IVDR-Vorgaben, damit Ihre Geräte sicher und effizient eingesetzt werden können.
Was uns besonders auszeichnet
ISO 13485-zertifiziert
Unser Qualitätsmanagementsystem ist gemäß ISO 13485 zertifiziert. Damit gewährleisten wir eine konforme Entwicklung von Software für In-vitro-Diagnostika und erfüllen die Anforderungen der IVDR an Qualitätsmanagementsysteme.
Externe Inverkehrbringung
Auf Wunsch übernehmen wir für Ihr IVDR-Softwareprodukt die Rolle des legalen Herstellers. Wir tragen die rechtliche Verantwortung für die Einhaltung aller regulatorischen Anforderungen der IVDR, sodass Sie sich auf Ihre Kernkompetenzen wie Vertrieb und Vermarktung konzentrieren können.
ISO 27001-zertifiziert
QuickBird Medical ist nach ISO 27001 für Informationssicherheit zertifiziert. Wir sind Experten in den Bereichen Cybersecurity und Datenschutz, speziell für Gesundheitsdaten.
Planen Sie die Entwicklung eines Software-Produkts für In-vitro-Diagnostika?
Unser Team unterstützt Sie bei der Planung und technischen Umsetzung Ihrer IVD-Software. Profitieren Sie von unserer Erfahrung in der Implementierung der regulatorischen Anforderungen der Verordnung über In-vitro-Diagnostika (IVDR). Kontaktieren Sie uns und vereinbaren Sie ein unverbindliches Erstgespräch. Gemeinsam finden wir heraus, wie wir Sie bei Ihrem Projektvorhaben unterstützen können.