Stand Januar 2024
In Belgien wurde neben Deutschland und Frankreich ein spezieller Zulassungsprozess für digitale Gesundheitsanwendungen etabliert. Auch in Österreich gibt es seit 2020 stärker werdende Bestrebungen, DiGA in die reguläre Gesundheitsversorgung zu integrieren. Mit Blick auf die beiden Vorreiterländer wurde das große Potenzial für eine patientenzentrierte medizinische Versorgung festgestellt und daher ein spezieller Zulassungspfad geschaffen: die mHealth-Pyramide. Mit dieser soll der belgischen Bevölkerung der Zugang zu qualitätsgeprüften und wirksamen digitalen Gesundheitsanwendungen gegeben werden.
Wir werfen in diesem Artikel einen detaillierten Blick auf die Schritte des Zulassungsprozesses und Sie erfahren, welche Anforderungen es zu beachten gilt, um erstattungsfähige digitale Gesundheitsanwendungen erfolgreich in Belgien einzuführen.
Darüber hinaus nimmt dieser Artikel auch die Unterschiede und Ähnlichkeiten zwischen dem deutschen DiGA-Fast-Track und der belgischen mHealth-Pyramide unter die Lupe: Durch den Vergleich beider Ansätze erhalten Sie einen umfassenden Überblick über die verschiedenen Wege, die die beiden Länder eingeschlagen haben, um digitale Gesundheitsanwendungen zu fördern.
Ein besonderer Fokus wird dabei auf der Möglichkeit zur vorläufigen Zulassung mit Analogie zum deutschen DiGA-Fast-Track liegen.
Inhaltsverzeichnis
- 1. Zulassung innerhalb der mHealth-Pyramide
- 2. Der belgische Zulassungsprozess für Stufe 3 der mHealth-Pyramide
- 2.1 Kriterien für eine Zulassung auf Stufe 3
- 2.2 Antragsverfahren beim NIHDI/ INAMI
- 2.3 Ablauf der Bewertung zur vorläufigen Zulassung
- 2.4 Ablauf der Bewertung zur dauerhaften Zulassung
- 2.5 Schlüsselaspekte für nicht-belgische Antragsteller
- 2.6 Wer darf einen Antrag stellen?
- 2.7 Welche digitalen Gesundheitsanwendungen werden bisher vom NIHDI erstattet?
- 3. Übersicht: mHealth Stufe 3 versus DiGA-Fast-Track
- 4. DiGA-Modelle in anderen Ländern
- 5. Fazit
1. Zulassung innerhalb der mHealth-Pyramide
Zuerst werfen wir einen Blick auf die mHealth-Pyramide, um eine grobe Übersicht über das belgische Konzept hinsichtlich Struktur, Verantwortlichkeiten und Anforderungen zu erhalten.
Sie bildet seit 2021 den Zulassungsprozess für vielfältige digitale Anwendungen ab, von der Videosprechstunde bis zu digitalen Gesundheitsanwendungen. Der offizielle Titel dieser digitalen Lösungen ist „Applications de santé mobiles“ oder „Applications mobiles médicales“. Dabei handelt es sich nicht ausschließlich um Apps für die Nutzung auf Smartphones. Auch reine Desktop-Anwendungen für medizinisches Fachpersonal führt mHealthBELGIUM in der Liste der Softwarelösungen auf.
1.1 Aktueller Stand des belgischen Zulassungsprozesses
Die mHealth-Pyramide und der damit verbundene rechtliche Rahmen für die Finanzierung von medizinischen Apps wurde 2016 entwickelt. Beides wurde im Januar 2021 abgeschlossen und liegt als königlicher Erlass vor. Da es sich noch um ein neues Verfahren im belgischen Gesundheitssystem handelt, sind in Zukunft noch Anpassungen erwarten.
Eine Liste der digitalen Gesundheitsanwendungen findet sich auf der Website von mHealthBELGIUM. Das Verzeichnis wird allerdings nur in unregelmäßigen Abständen aktualisiert.
1.2 Aufbau der mHealth-Pyramide
Die mHealth-Pyramide in Belgien ist in drei Stufen mit zunehmend strengeren Anforderungen aufgebaut und erfordert die Interaktion mit unterschiedlichen öffentlichen Stellen. Dieses Stufensystem wurde für ein breites Spektrum digitaler Gesundheitslösungen konzipiert.
Die untenstehende Abbildung der Pyramide soll eine erste Orientierung für die darauffolgende Erläuterung geben. Auf der linken Seite sind in groben Zügen die Anforderungen ausgewiesen, die auf der jeweiligen Stufe erfüllt werden müssen. Auf der rechten Seite sind die involvierten Institutionen aufgeführt.
Von besonderem Interesse sind im weiteren Verlauf des Artikels die blau hervorgehobenen Stufen „3-“ und „3+“: Sofern eine digitale Gesundheitsanwendung die Anforderungen dieser Stufen erfüllt, wird sie von den belgischen Krankenkassen erstattet.
 Zulassung im Rahmen der mHealth-Pyramide in Belgien
Zulassung im Rahmen der mHealth-Pyramide in Belgien
1.3 Das Stufensystem der mHealth-Pyramide
Eine digitale Anwendung muss, sobald sie ein CE-Kennzeichen als Medizinprodukt trägt, verpflichtend auf einer der Stufen der mHealth-Pyramide zugelassen werden, um in Belgien auf den Markt gebracht zu werden. Die grundlegende klinische Wirksamkeit und Sicherheit sind also bereits an diesem Punkt gesichert.
Eigenschaften und Zweck Ihres Produkts sowie Ihr Zielvorhaben mit der Zulassung beeinflusst die Stufe, die Sie wählen:
- Für digitale Gesundheitsanwendungen, die lediglich Gesundheitsdaten sammeln und an medizinisches Fachpersonal übertragen, reicht dabei eine Zulassung auf Stufe 1.
- Sobald die Anwendung eine Funktion zur aktiven Überwachung von Gesundheitszuständen oder Diagnosefunktionen aufweist, muss die Anwendung die Kriterien der Stufe 2 erfüllen.
- Eine Zulassung auf Stufe 3 ist dann stets freiwillig und wird vom Antragsteller nur angestrebt, wenn die Gesundheitsanwendung von den belgischen Krankenkassen erstattet werden soll.
Da die Stufen aufeinander aufbauen, werden sie, falls erforderlich, nacheinander durchlaufen: Die Nachweise aus einer Stufe werden für die Zulassung auf der nächsten Stufe benötigt.
Mehr Informationen zu den einzelnen Stufen finden Sie in der folgenden Tabelle:
| Zulassungsbedingung | zuständige Stelle |
Vergütungsmöglichkeit
|
|
| Stufe 1 |
|
FAHMP (Bundesagentur für Arzneimittel und Gesundheitsprodukte) |
individuelle Vereinbarungen mit Kliniken oder Krankenkassen |
| Stufe 2 |
|
FAHMP (Bundesagentur für Arzneimittel und Gesundheitsprodukte) Koordination über die sogenannte eHealth-Plattform an der verschiedene Institutionen mitwirken |
individuelle Vereinbarungen mit Kliniken oder Krankenkassen |
| Stufe 3 |
|
NIHDI (Nationales Institut für Kranken- und Invalidenversicherung) |
Vergütung durch die Krankenkassen (vorläufig oder dauerhaft)
|
2. Der belgische Zulassungsprozess für Stufe 3 der mHealth-Pyramide
Im Folgenden konzentrieren wir uns auf die Anforderungen für die Zulassung einer digitalen Gesundheitsanwendung auf Stufe 3. Sowohl die Analogien als auch die Unterschiede zum deutschen DiGA-Fast-Track-Verfahren werden hier deutlich. Untenstehend finden Sie außerdem einen tabellarischen Vergleich zwischen dem deutschen und belgischen Prozess für die Zulassung digitaler Gesundheitsanwendungen.
2.1 Kriterien für eine Zulassung auf Stufe 3
Zuständig für den Antragsprozess ist das NIHDI. Es heißt mit vollem Namen Nationales Institut für Kranken- und Invalidenversicherung und hat eine Vielzahl an Aufgaben im belgischen Gesundheitssystem. Es firmiert auch unter der französischen Abkürzung INAMI.
Entscheidend für die Finanzierung digitaler Gesundheitsanwendungen durch die belgischen Krankenkassen sind folgende Punkte:
- Erfüllung der Kriterien aus Stufe 1 und 2
- Integration in ein Versorgungskonzept: Schlüsselelement, um den gesundheitsökonomischen Mehrwert nachzuweisen
- Klinische Wirksamkeit
- Gesundheitsökonomischer Mehrwert: Die App führt beispielsweise zu Verbesserungen in der Patientenversorgung, Kosteneinsparungen oder anderen Vorteilen.
Für eine vorläufige Zulassung auf Stufe „3-„ müssen die Nachweise aus den Punkten 2. bis 4. noch nicht erbracht sein. Es müssen jedoch Nachweiskonzepte mit den Antragsunterlagen eingereicht werden. Dies kann zum Beispiel ein Studiendesign sein.
2.2 Antragsverfahren beim NIHDI/ INAMI
Antragsteller entscheiden sich zuerst, ob sie eine vorläufige oder direkt eine dauerhafte Erstattung durch das NIHDI beantragen möchten und stellen das Dossier mit den notwendigen Unterlagen dementsprechend zusammen.
Ähnlich wie im deutschen BfArM kommt zur Bewertung des Antrags ein multidisziplinärer Ausschuss zusammen. Derzeit umfasst das Gremium 13 Personen aus verschiedenen Interessensgruppen wie Krankenkassen, Patientenvertretern oder Mitgliedern des NIHDI.
2.3 Ablauf der Bewertung zur vorläufigen Zulassung
Der Ausschuss bewertet den eingegangenen Antrag auf Vollständigkeit und berät in üblicherweise drei Sitzungen über die Möglichkeit der vorläufigen Erstattung.
Möglichkeiten zur Ablehnung bestehen an allen Stellen des Verfahrens:
- wenn die Antragsunterlagen nicht vollständig sind.
- wenn die vorläufige Erstattung abgelehnt wird.
- wenn die eingereichten Nachweise für eine dauerhafte Erstattung als ungenügend angesehen werden.
Hersteller haben während der Entscheidungsfindung des Gremiums die Möglichkeit, das Antragsdossier persönlich zu erläutern und auf Nachfragen zu reagieren.
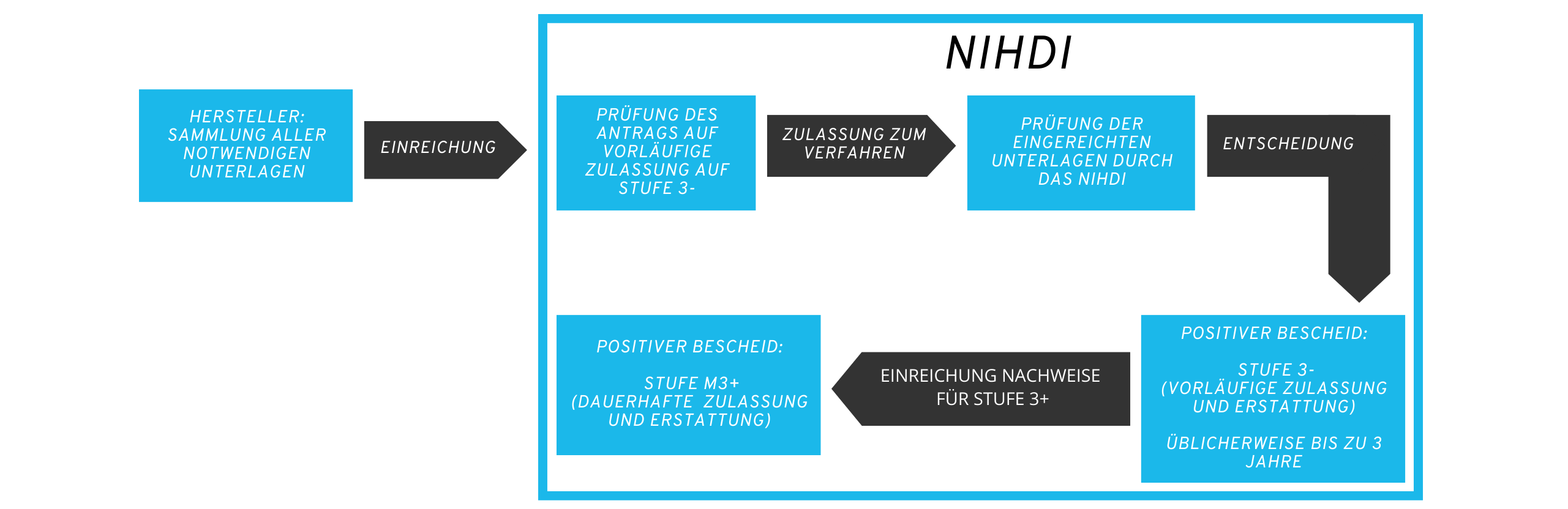
Belgien – Der Weg von der vorläufigen zur dauerhaften Erstattung durch das NIHDI
Die Dauer der vorläufigen Zulassung beträgt üblicherweise drei Jahre. In dieser Zeit wird die Gesundheitsanwendung bereits von den Krankenkassen erstattet. Der Preis wird vom Antragsteller mit dem NIHDI verhandelt.
Zum Vergleich: In Deutschland beträgt die standardmäßige vorläufige Erstattungsdauer nur 1 Jahr. Außerdem wird der Preis während der vorläufigen Zulassung in Deutschland vom Hersteller festgelegt. Erst wenn die DiGA dauerhaft erstattet werden soll erfolgt eine Preisverhandlung zwischen Hersteller und GKV-Spitzenverband.
Während der Phase der vorläufigen Erstattung muss der Antragsteller nach 18 Monaten an das NIHDI über den Fortschritt des Umsetzungsplans zur endgültigen Zulassung berichten. Die vollständigen Unterlagen für den Entscheid über die dauerhafte Zulassung und Erstattung müssen spätestens 6 Monate vor dem Ende des Erprobungszeitraumes vorliegen.
2.4 Ablauf der Bewertung zur dauerhaften Zulassung
Entscheiden sich Antragsteller direkt die dauerhafte Zulassung zu beantragen, so werden von Anfang an alle Unterlagen von einer Arbeitsgruppe des NIHDI auf Vollständigkeit geprüft und dem Antragsteller am Ende ein Bescheid erteilt.
Dies bedeutet, dass sämtliche Nachweise über
- die klinische Wirksamkeit,
- den positiven sozioökonomischen Effekt,
- und die erfolgreiche Einbindung in einen Versorgungsprozess
schon vor Antragstellung vollständig vorliegen müssen.
In Belgien ist zum Veröffentlichungszeitpunkt dieses Blog-Artikels noch kein direkter Antrag auf dauerhafte Zulassung gestellt worden. Praxisbeispiele dazu fehlen also bisher.
2.5 Schlüsselaspekte für nicht-belgische Antragsteller
Für eine erfolgreiche Zulassung einer digitalen Gesundheitsanwendung beim NIHDI ist ein fundiertes Verständnis des belgischen Gesundheitssystems von Vorteil, da einige Besonderheiten zu beachten sind. Im Vergleich mit dem deutschen DiGA-Fast-Track Verfahren fallen diese Unterschiede auf, die sich explizit auf die Einbettung der Argumentation in den Kontext des belgischen Gesundheitssystems beziehen:
- Integration in einen Versorgungspfad
Im Gegensatz zu deutschen DiGA können digitale Gesundheitsanwendungen immer nur als integriert in einen innovativen Versorgungspfad zugelassen und auch vergütet werden. Dieses Kriterium hat keine exakte Entsprechung im deutschen DiGA-Fast-Track.
Diese Integration gelingt nicht ohne Partnerschaften im belgischen Gesundheitssystem. Hersteller können mit Gesundheitseinrichtungen, wie Krankenhäusern und Arztpraxen, zusammenarbeiten, um die Anwendung in bestehende Versorgungsprozesse zu integrieren. Pilotstudien sind eine Möglichkeit, die erfolgreiche Integration nachzuweisen. Über User-Feedback oder Erfahrungsberichte von medizinischem Fachpersonal können die Vorteile der Behandlung dokumentiert werden. Gegebenenfalls können auch Aspekte einer klinischen Studie die gelungene Integration in die belgische Versorgungslandschaft nachweisen.
Für die Erfüllung dieses zusätzlichen Kriteriums sind gute Kontakte zu Akteuren im belgischen Gesundheitssystem wichtig.
- Klinische Wirksamkeit
Für den Zulassungsantrag in Belgien kann der Nachweis der klinischen Wirksamkeit durch eine Studie aus dem Ausland, wie beispielsweise aus Deutschland für eine DiGA, verwendet werden. Das Produkt hat bereits durch die CE-Kennzeichnung als Medizinprodukt Nachweise für Sicherheit und Wirksamkeit erbracht. Es muss jedoch unter anderem plausibel begründet werden, warum dieser Nachweis auch für das belgische Gesundheitssystem gültig ist. Eine Bezugnahme auf die belgische Population und der Nachweis der Übertragbarkeit der Studienergebnisse sind unerlässlich.
- Gesundheitsökonomischer Effekt:
Auch beim Nachweis des gesundheitsökonomischen Effekts gelten ähnliche Bedingungen. Während in Deutschland der Fokus bei DiGA stark auf der Verbesserung der Patientenversorgung liegt, betont Belgien zusätzlich die Bedeutung von Prozessverbesserungen im Gesundheitswesen. Ein Beispiel dafür könnte die Verringerung postoperativer Komplikationen oder eine effizientere Patientenbetreuung sein.
Argumente aus bestehenden Unterlagen einer DiGA-Zulassung in Deutschland sind nur hilfreich, wenn sie nachweisen können das das vorgestellte Versorgungskonzept sowohl innovativ als auch den bestehenden belgischen Konzepten überlegen ist.
2.6 Wer darf einen Antrag stellen?
Seit Oktober 2023 haben nicht nur die Hersteller, sondern auch verschiedene andere Akteure in Belgien die Möglichkeit, in Zusammenarbeit mit den Herstellern Anträge für die Zulassung digitaler Gesundheitsanwendungen zu stellen. Dazu zählen Vertriebsunternehmen, Krankenhäuser, wissenschaftliche Verbände oder Berufsverbände.
Beispielsweise können Kliniken, die innovative Versorgungskonzepte einführen wollen und dabei auf digitale Gesundheitsanwendungen als Bausteine setzen, ebenfalls Anträge beim NIHDI stellen.
Beim NIHDI stehen die jeweiligen Antragsformulare zur Verfügung.
Beispiele aus der Praxis fehlen hierfür bisher. Die erweiterte Möglichkeit zur Antragstellung wird nach einem Jahr vom NIHDI bewertet. Es ist daher in Zukunft mit Anpassungen zu rechnen.
2.7 Welche digitalen Gesundheitsanwendungen werden bisher vom NIHDI erstattet?
Zum Veröffentlichungszeitpunkt dieses Blog-Artikels werden lediglich die drei Anwendungen des Herstellers moveUP erstattet.
Eine davon ist die Smartphone-App moveUP, die zur Rehabilitation nach Knie- oder Hüftoperationen verwendet wird. Sie schlägt aufgrund der Informationen personalisierte Übungen vor und überträgt die von den Patienten eingegebenen Informationen an die behandelnden Ärzte.
Am Beispiel von moveUP wird deutlich, wie bedeutend die Integration in einen Versorgungspfad und der daraus resultierende sozioökonomische Nutzen sind.
moveUP wurde von Anfang an nicht isoliert entwickelt, sondern als integraler Bestandteil eines Versorgungspfades, der sowohl für die Klinik als auch für die Patienten Vorteile bietet.
- Smartphone App für Patienten: In der Smartphone-App moveUP erhalten Patienten auf sie abgestimmte Übungen für die Rehabilitation nach einer Knie- oder Hüft-OP. Außerdem beantworten sie Fragen zu ihrem Gesundheitszustand. Die Daten werden an die behandelnden Ärzte übermittelt.
- Desktopanwendung für Ärzte: Auf ärztlicher Seite steht eine Desktopanwendung zur Übertragung und Auswertung der Daten zur Verfügung, die die Patienten in der Smartphone-App move Up erfassen.
- Coaching- System: Es gibt in der mobilen App eine Anbindung an ein Coaching-System, in welchem den Patienten Fragen direkt durch medizinisches Personal beantwortet werden. Dadurch muss die Arztpraxis nicht für kleinere Anliegen aufgesucht werden.
Durch die Bereitstellung dieser drei Anbindung entsteht der neue Versorgungspfad.
3. Übersicht: mHealth Stufe 3 versus DiGA-Fast-Track
Für einen besseren Überblick werden hier noch einmal die wesentlichen Elemente der Zulassungswege in Belgien und Deutschland miteinander verglichen.
Ähnlichkeiten der Stufe 3 der mHealth Pyramide mit dem deutschen DiGA-Fast-Track Verfahren
| Stufe 3 der mHealth-Pyramide |
Deutscher DiGA-Fast-Track
|
|
| zuständige Behörde |
NIHDI |
BfArM |
| Zulassungssystem |
Stufe 3 mit Ähnlichkeiten zum deutschen DiGA-Fast-Track |
DiGA Fast-Track-Prozess |
| Zielgruppe |
Apps mit therapeutischer und/oder diagnostischer Funktion |
Apps mit therapeutischer und/oder diagnostischer Funktion |
| Möglichkeit zur vorläufigen Zulassung |
ja üblicherweise für 3 Jahre |
ja für 1 Jahr, Verlängerung um 1 Jahr möglich in Einzelfällen |
| Nachweis positiver Versorgungseffekt |
verpflichtend für dauerhafte Zulassung |
verpflichtend für dauerhafte Zulassung |
| Erstattungsmechanismus |
durch die Krankenkassen |
durch die Krankenkassen |
Unterschiede der Stufe 3 der mHealth Pyramide mit dem deutschen DiGA-Fast-Track Verfahren
| Stufe 3 der mHealth-Pyramide |
Deutscher DiGA-Fast-Track
|
|
| mögliche Antragsteller |
|
Hersteller |
| zugelassene Risikoklassen nach MDR |
alle |
I-IIa (zukünftig auch IIb) |
| Preisverhandlungen |
|
|
| Nachweis sozioökonomischer Effekt |
vorgeschrieben |
nein |
| Integration in bestehende Versorgungspfade |
vorgeschrieben |
nein Eine DiGA kann alleinstehend verordnet werden. |
| Rezept notwendig für die Nutzung der App? |
teilweise |
ja |
| Verzeichnis aller zugelassenen Apps |
inaktuelles Verzeichnis von mHealthBELGIUM |
DiGA-Verzeichnis des BfArM |
4. DiGA-Modelle in anderen Ländern
Immer mehr Länder planen einen standardisierten Prozess, um digitale Gesundheitsanwendungen in die Regelversorgung zu bringen. Neben Belgien sollten Sie außerdem einen Blick in die folgenden Länder werfen:
- DiGA in Deutschland
- DiGA in Frankreich
- DiGA in der Schweiz
- DiGA in Österreich
- DiGA in Italien
- Überblick über Zulassung von DiGA in allen Ländern der EU
Außerdem gibt es eine breite Palette von öffentlichen Förderungen (siehe unser Praxisleitfaden zu Digital Health-Förderungen) und anderen Erstattungswegen (siehe unser Whitepaper zu Selektivverträgen) für Health-Software.
5. Fazit
Belgien zeigt sich in vielen Bereichen des Gesundheitssystems sehr aufgeschlossen gegenüber der Digitalisierung, was sich unter anderem in der Existenz der elektronischen Patientenakte und der Gewöhnung der Bürger an digitale Versorgungsprozesse widerspiegelt.
Dies schafft für Hersteller digitaler Gesundheitsanwendungen einen attraktiven Markt in einem digitalisierungsfreundlichen Umfeld.
Die pragmatische Herangehensweise der belgischen Behörden bei der Zulassung von Gesundheitsapps kann sowohl vorteilhaft als auch herausfordernd sein. Einerseits ist somit in kurzer Zeit ein neuer Zulassungsprozess geschaffen worden. Andererseits sind einige Anforderungen zum aktuellen Zeitpunkt noch nicht klar definiert und es ist mit weiteren Anpassungen zu rechnen. Diese dynamische Situation sorgt für Unsicherheit bei Herstellern.
Wenn Sie die Zulassung einer digitalen Gesundheitsanwendung in Belgien planen, kontaktieren Sie uns gerne. Wir helfen Ihnen die Anwendung zu entwickeln und den optimalen Zulassungspfad zu finden.