Was bringt schon eine DiGA, die das Leben von Patienten nicht verbessert? Gar nichts!
Deshalb erhalten DiGA auch erst Ihre Daseinsberechtigung, wenn ihr positiver Versorgungseffekt nachgewiesen werden konnte. Erst dann haben Sie eine Chance, dauerhaft ins Verzeichnis des BfArM aufgenommen zu werden. Am Ende soll Ihre DiGA schließlich einen echten Mehrwert für den Patienten liefern. Denn auch Krankenkassen wollen nur für Maßnahmen bezahlen, die einen Nutzen haben.
In diesem Artikel geben wir Ihnen einen detaillierten Leitfaden darüber, wie der Nachweis positiver Versorgungseffekte zu erfolgen hat.
Inhalt
- 1. Was ist ein positiver Versorgungseffekt?
- 2. Notwendige Angaben im Antrag
- 3. Studie zum Nachweis positiver Versorgungseffekte
- 4. Evaluationskonzept (bei vorläufiger Aufnahme)
- 5. Zusammenfassung
1. Was ist ein positiver Versorgungseffekt?
Ein positiver Versorgungseffekt kann viele Gesichter haben. Das merken wir beispielsweise, wenn wir uns einen typischen Behandlungsverlauf bei einer Depression ansehen:
- Niedergeschlagenheit und andere depressive Symptomatik
- Erstbesuch beim Hausarzt
- Stellung einer Verdachtsdiagnose
- Überweisung zu einem Psychotherapeuten
- Wartezeit von 6 Monaten (Quelle: BR24)
- Diagnostik & Diagnosestellung
- Ambulante Psychotherapie (20 – 25 Wochen)
- Rückfallprophylaxe
Schon in dieser sehr vereinfachten Darstellung wird deutlich, in welchen Bereichen die Versorgung von Patienten verbessert werden kann. Dazu gehört nicht nur die Optimierung der Therapie, sondern auch die Verbesserung von strukturellen Parametern, wie etwa eine Verkürzung der Wartezeit oder die Stärkung der Rolle des Patienten in der Therapie. Grundsätzlich unterscheidet die DiGA-Verordnung (DiGAV) beim positiven Versorgungseffekt zwischen zwei großen Kategorien: medizinischer Nutzen und patientenrelevante Struktur- und Verfahrensverbesserungen.
1.1 Medizinischer Nutzen
Im Grunde ist ein medizinischer Nutzen jede Form der Verbesserung von Diagnostik und Therapie. Konkret sind folgende vier Kategorien in der DiGAV als medizinischer Nutzen definiert:
- Verbesserung des Gesundheitszustands
- z.B. Rückgang von Symptomen
- Verkürzung der Krankheitsdauer
- z.B. Schnellere Rehabilitation nach einer OP
- Verlängerung des Überlebens
- z.B. Frühere Erkennung von Herzerkrankungen
- Verbesserung der Lebensqualität
- z.B. besserer Umgang mit einer Erkrankung
QuickBird Medical Tipp: Wie man in unserem DiGA-Verzeichnis-Analyzer sieht, gibt es aktuell (Nov 2025) keine im Verzeichnis gelistete DiGA, die nicht einen medizinischen Nutzen nachgewiesen hat. Eine DiGA mit einem reinen strukturellen Effekt (pSVV – siehe nächstes Kapitel) hat generell schlechte Chancen auf eine Listung im DiGA-Verzeichnis. Sie sollten sich auf den medizinischen Nutzen fokussieren, um Ihre Erfolgswahrscheinlichkeit zu maximieren. Mehr Infos finden Sie in unserem DiGA-Verzeichnis-Analyzer: Link
1.2 Patientenrelevante Struktur- und Verfahrensverbesserung (pSVV)
Wie eingangs erwähnt, muss eine DiGA nicht zwangsläufig bei der Therapie oder Diagnostik einer Erkrankung unterstützen, um einen positiven Versorgungseffekt zu erzielen. Auch organisatorische Verbesserungen, wie etwa die Verkürzung von Wartezeiten oder ein einfacherer Zugang zu medizinischen Leistungen wird nach DVG als positiver Versorgungseffekt gewertet. Der pSVV unterteilt sich gemäß DiGAV §8, Absatz 3 in folgende Aspekte:
- Koordination von Behandlungsabläufen
- Eine DiGA kann beispielsweise die Koordination zwischen dem Patienten und mehreren Leistungserbringern (z.B. Psychotherapeut und Neurologe) optimieren, um einen besser organisierten Therapieablauf zu ermöglichen.
- Ausrichtung der Behandlung an Leitlinien und anerkannten Standards
- Umsetzung von Patientenleitlinien in Apps, um Betroffenen zu verdeutlichen, wie sie selbst an der Behandlung mitwirken können. Eine App könnte beispielsweise gesundheitsrelevante Informationen anzeigen und regelmäßig an notwendige Arzttermine erinnern.
- Adhärenz
- Unterstützung bei der Umsetzung von Maßnahmen, die gemeinsam mit dem Arzt vereinbart wurden. Dadurch soll der Patient in seiner aktiven Rolle bestärkt werden.
- Erleichterung des Zugangs zur Versorgung
- DiGA können dazu beitragen, den Zugang zu medizinischer Versorgung zu verbessern und somit Barrieren, wie den Wohnort oder andere Faktoren kompensieren.
- Patientensicherheit
- Im Vordergrund steht hier die Vermeidung von Behandlungsfehlern. DiGA können diesen vorbeugen oder den Patienten dabei unterstützen, Fehler selbst zu erkennen.
- Gesundheitskompetenz
- Menschen fällt es oft schwer, gesundheitsrelevante Informationen zu finden und zu interpretieren. DiGA können dieses Wissen gezielt transferieren und Patienten ein größeres Verständnis für ihre Erkrankung und die Therapie ermöglichen.
- Patientensouveränität
- DiGA können Patienten darin bestärken, an den Entscheidungsprozessen in der Behandlung mitzuwirken und seine Erfahrungen miteinfließen zu lassen.
- Bewältigung krankheitsbedingter Schwierigkeiten im Alltag
- Hier geht es um die Unterstützung bei der Kompensation und der Reduktion von Unsicherheiten im Alltag. Eine Anwendung kann dafür sorgen, dass sich ein Patient frühzeitig auf ein Symptom einstellen kann oder ihn bei alltäglichen Tätigkeiten unterstützen.
- Reduzierung der therapiebedingten Aufwände und Belastungen der Patienten und ihrer Angehörigen
- Viele Therapien sind mit großen Aufwänden seitens der Patienten verbunden. Eine App kann hier beispielsweise helfen, indem sie Wartezeiten verkürzt oder sinnvoll überbrückt oder die physische Anwesenheit bei Terminen minimiert.
Sieht man sich die verschiedenen Bereiche an, merkt man schnell, dass es pSVV vor allem darum geht, die Rolle des Patienten in seiner eigenen Versorgung zu stärken.
Ökonomische Aspekte werden hier bewusst nicht berücksichtigt. Wenn Ihre DiGA den Patienten und Krankenkassen finanzielle Erleichterungen ermöglicht, ist das ein gutes Argument für Ihre Preisverhandlungen, gilt aber nicht als positiver Versorgungseffekt.
QuickBird Medical Tipp: Da eine DiGA als Medizinprodukt zertifiziert sein muss, muss sie laut MDR auch eine Form von diagnostischem oder therapeutischen Nutzen haben. Das hat zur Folge, dass manche Anwendungen, die nur einen pSVV bewirken, nicht als Medizinprodukt gelten und somit auch keine DiGA werden können.
Lesen Sie hier mehr über die Zweckbestimmung nach MDR und die Voraussetzungen für Medizinprodukte.
2. Notwendige Angaben im Antrag
Egal, ob Sie einen Antrag auf dauerhafte oder vorläufige Listung im DiGA-Verzeichnis stellen – einige Angaben sind für alle Hersteller obligatorisch.
2.1 Angabe der Patientengruppe
Sie müssen angeben, für welche Patientengruppe ein positiver Versorgungseffekt erzielt werden soll. Dafür ist ausschließlich eine Eingrenzung nach ICD-Codes zulässig. Jeder ICD-Code beschreibt eine Diagnose, wobei sowohl drei- als auch vierstellige Codes zulässig sind. Dreistellige Codes umfassen eine breitere Patientengruppe, wohingegen ein vierstelliger Code eine nähere Spezifikation dieser Patientengruppe darstellt.

Bedeutung von ICD-Codes
Beispiel:
- Dreistelliger Code:
- F32 = Depressive Episode
- Vierstelliger Code:
- F32.0 = Leichte depressive Episode
- F32.1 = Mittelgradige depressive Episode
Falls Ihre DiGA bei mehreren Indikationen einen positiven Versorgungseffekt nachweisen soll, müssen Sie für jede Patientengruppe einen Nachweis erbringen. Sie können den Nutzen aber auch gleichzeitig für mehrere Indikationen nachweisen, wenn er im Wesentlichen für diese vergleichbar ist. Dazu müssen Sie aber auch alle Indikationen in Ihre Studie mit einbeziehen. Die finale Bewertung, ob der angestrebte Versorgungseffekt dann auch für alle Gruppen vorliegt, obliegt dem BfArM.
Achtung: Ihre DiGA kann am Ende auch nur bei den Indikationen verschrieben werden, für die Sie auch einen Nutzennachweis erbringen können. Definieren Sie in Ihrem Antrag beispielsweise nur F32.1 als Patientengruppe, kann ein Arzt oder Psychotherapeut die DiGA nicht an Patienten verschreiben, denen ein F32.0 (leichte depressive Episode) attestiert wird.
2.2 Angabe des positiven Versorgungseffekts
Eine DiGA muss mindestens einen positiven Versorgungseffekt nachweisen können. Zentral ist hierbei, dass dieser auch konsistent mit der Zweckbestimmung, den Funktionen und Inhalten der DiGA und den veröffentlichten Aussagen (z. B. in Werbematerial) ist. Daher sollten Sie sich zeitgleich mit der Medizinprodukt-Zertifizierung bereits an den Nachweis des positiven Versorgungseffekts denken.
Eine Zweckbestimmung kann nicht mehr so einfach geändert werden. Achten Sie also darauf, dass diese nicht allzu spezifisch formuliert ist. Sie wollen ja später nicht das Potenzial Ihrer DiGA verschenken, wenn diese z.B. auch für andere Indikationen geeignet ist.
QuickBird Medical Tipp: Ein Nachweis mehrerer positiver Versorgungseffekte kann einen großen Mehrwert für die späteren Preisverhandlungen schaffen. Hier erfahren Sie mehr über die Preisverhandlung mit dem GKV-Spitzenverband.
3. Studie zum Nachweis positiver Versorgungseffekte
Der Nachweis eines positiven Versorgungseffekts liefert die Daseinsberechtigung für jede DiGA. Selbstverständlich handelt es sich daher auch um eines der wichtigsten Dokumente, das dem BfArM vorgelegt werden muss. Beim Studiendesign gibt es klare Vorgaben, welche wir in diesem Kapitel behandeln.
Der Durchführungsort der Studie muss Deutschland sein. Denkbar sind zwar auch Länder, in denen das Gesundheitssystem mit dem deutschen vergleichbar ist – dies birgt allerdings große Mehraufwände und Sie müssen genau begründen, warum hier eine Vergleichbarkeit vorliegt.
Zudem muss die Studie auch in einem öffentlichen Studienregister eingetragen werden. Das anerkannte Primärregister für Deutschland ist das Deutsche Register klinischer Studien (DRKS) beim BfArM.
12 Monate nach Einreichung der Studienergebnisse beim BfArM muss die Studie auch veröffentlicht werden. Dabei ist eine Veröffentlichung auf der Webseite ausreichend.
Wenn Sie für die Zertifizierung als Medizinprodukt nach MDR im Zuge der klinischen Bewertung eine Studie durchführen müssen, sollten Sie in Betracht ziehen, diese auch direkt auf die Anforderungen des BfArM abzustimmen. Wenn Sie dabei sauber vorgehen, können Sie mit einer Studie sowohl die klinische Prüfung nach MDR durchführen als auch den positiven Versorgungseffekt nachweisen.
QuickBird Medical Tipp: Buchen Sie unbedingt ein Beratungsgespräch beim BfArM, um Ihr Studiendesign bzw. Studiensynopse vorab zu besprechen. Auch wenn Sie von Qualität Ihrer geplanten Studie überzeugt sind, kann das BfArM hier eine andere Meinung haben. Am Ende zählt die Meinung des BfArM bei der Zulassung.
3.1 Zulässige Studientypen
Ein kurzes Experteninterview mit meinem Hausarzt sollte doch als Studie reichen, oder? Nein, so einfach geht das nicht.
Anwendungen im DiGA-Verzeichnis werden von den Krankenkassen finanziert und flächendeckend von Patienten genutzt. Das BfArM hat daher ein starkes Interesse daran, dass zu diesen Produkten auch aussagekräftige Erkenntnisse vorliegen. Deshalb vertrauen sie ausschließlich quantitativen Untersuchungen, wie es in der klinischen Forschung üblich ist. Als Mindestanforderung gilt, dass es sich um eine vergleichende Studie handeln muss. Nur so kann ein aussagekräftiger Nutzennachweis erbracht werden.
Einfach gesagt: Sie vergleichen Patienten, die Ihre DiGA nutzen mit Patienten, die Ihre DiGA nicht nutzen.
Achtung: Es ist nicht gesagt, dass die Patienten, die Ihre DiGA nicht nutzen, keine Behandlung bekommen! Die Kontrollgruppe muss nämlich an der Versorgungsrealität orientiert sein und eine für ihre Situation übliche Behandlung erhalten. Schließlich wollen Sie nachweisen, dass Ihre DiGA den aktuellen Zustand verbessern kann.
Auch vergleichende Studientypen lassen sich noch einmal untergliedern. Beispiele hierfür sind Kohortenstudien, nicht-randomisierte- und randomisierte kontrollierte Studien.
QuickBird Medical Tipp: Randomisierte kontrollierte Studien haben eine sehr hohe Aussagekraft im Vergleich zu vielen anderen vergleichenden Studientypen. Dadurch sind Ihre Ergebnisse weniger angreifbar. Offiziell bringt die Wahl eines aussagekräftigen Studientyps keine Vorteile vonseiten des BfArM. Aktuell hat aber fast jede dauerhaft gelistete DiGA im Verzeichnis ihre positiven Versorgungseffekte mit einer randomisierten kontrollierten Studie nachgewiesen (Stand 14.06.2021).
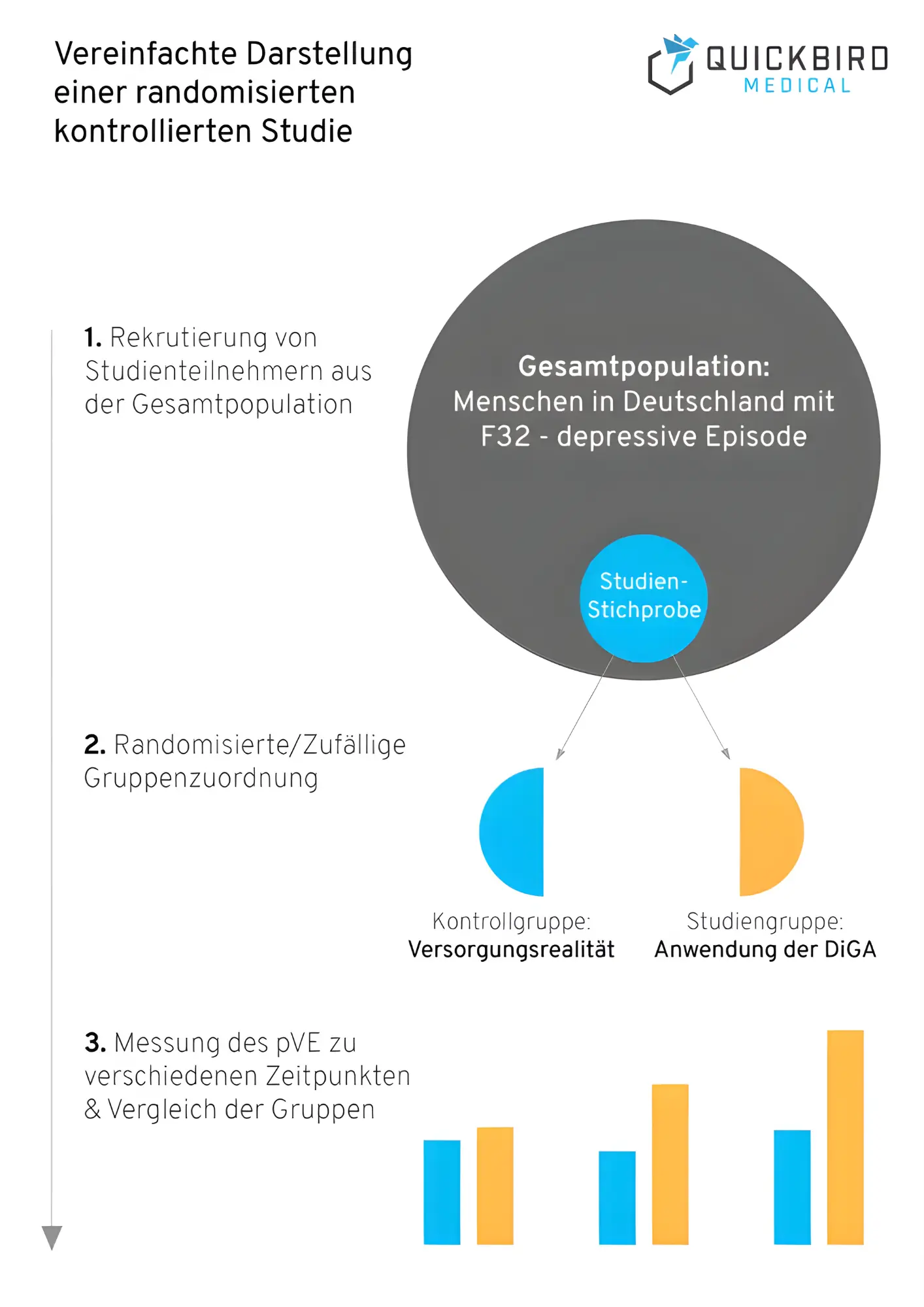
Vereinfachte Darstellung einer randomisierten kontrollierten Studie
Bei einer kontrollierten Studie werden die Teilnehmer in Gruppen unterteilt. Im einfachsten Fall handelt es sich dabei um eine Kontroll- und eine Studiengruppe. Es ist aber auch denkbar, mehrere Gruppen zu formen, um die Studienergebnisse besser einordnen zu können. Teilnehmer in der Studiengruppe werden in der Studie Ihre DiGA verwenden.
Wichtig ist, dass die Kontrollgruppe an der Versorgungsrealität orientiert ist. Wenn Menschen mit einer Indikation üblicherweise eine bestimmte Behandlung erhalten, sollten die Teilnehmer in Ihrer Kontrollgruppe diese Behandlung auch erhalten. Denn nur so ist eine realistische Nutzenbewertung möglich. Erhalten Menschen üblicherweise keine Behandlung (z.B. wegen Wartezeiten auf einen Therapieplatz), müssen auch Studienteilnehmer in der Kontrollgruppe keine Behandlung erhalten.
Beispiel: Ihre DiGA soll eine ambulante Psychotherapie bei Depression unterstützen, indem sie zusätzliche Empfehlungen liefert, die einen Patienten im Alltag unterstützen. Üblicherweise erhalten Patienten in diesem Szenario also eine ambulante Psychotherapie. Sie könnten Ihre Studienteilnehmer demnach in folgende Gruppen unterteilen:
- Gruppe 1: Patienten, die nur ambulante Psychotherapie erhalten
- Gruppe 2: Patienten, die ambulante Psychotherapie erhalten & zeitgleich die DiGA verwenden
Da es immer mehr DiGA gibt, die flächendeckend eingesetzt werden, ändert sich in manchen Bereichen auch die Versorgungsrealität. Ist die Behandlung mit einer anderen DiGA also bereits ein gängiges Vorgehen, müssen Sie Ihre DiGA in der Studie auch mit der bereits etablierten DiGA vergleichen.
Die Versorgungsrealität, die Sie in der Kontrollgruppe abbilden müssen, kann also drei Formen haben:
- Nichtbehandlung
- Behandlung ohne Einsatz bestehender DiGA
- Behandlung mit Einsatz bestehender DiGA
Ein zusätzliches Qualitätsmerkmal von Studien ist die Verblindung. Verblindung soll verhindern, dass Studienteilnehmer wissen, in welcher Gruppe sie sich befinden. Bei Medikamentenstudien erhält eine Studiengruppe dazu beispielsweise oft ein Placebo-Präparat, welches keine medizinische Wirkung hat. Bei der Untersuchung von Apps ist die Verblindung allerdings nur schwer umzusetzen.
3.2 Stichprobe
Die Stichprobe umfasst alle Teilnehmer, die Sie in Ihre Studie mit einbeziehen. All diese Teilnehmer müssen die Diagnose aufweisen, die Sie in ihrer Patientengruppe spezifizieren.
Ein großes Fragezeichen ist oft die Stichprobengröße. Im Zuge der Fallzahlplanung müssen Sie herausfinden und begründen, welche Stichprobengröße für die Studie optimal ist. Zu kleine Stichproben sind weniger repräsentativ und führen häufig dazu, dass existierende Effekte nicht erkannt werden. Zu große Stichproben sind für Sie als Hersteller natürlich teuer (Rekruitierung der Teilnehmer, Einschluss in die Studie etc.). Daher ist es wichtig hier eine möglichst präzise Prognose zu machen.
Die optimale Stichprobengröße wird im Rahmen einer statistischen Fallzahlplanung bestimmt. Dabei werden Annahmen über den erwarteten Effekt, die Streuung der Messwerte sowie das gewünschte Signifikanzniveau und die Power getroffen, um die notwendige Anzahl an Teilnehmern zuverlässig zu berechnen. Grundlage dafür sind mathematische Modelle und sofern verfügbar Parameter aus Pilotstudien oder der Literatur. Ein Statistiker übernimmt diese Planung üblicherweise.
Es ist auch möglich, für die Studie bereits existierende Daten zu verwenden (z.B. Abrechnungsdaten von Krankenkassen). Dadurch müssten Sie die Kontrollgruppe nicht selbst abbilden, ist allerdings oft mit erheblichen Aufwänden verbunden und erfordert gute Argumentation beim BfArM. Dabei müssen Sie sich außerdem auf die bereits gemessenen Endpunkte beschränken und sicherstellen, dass diese auch valide gemessen wurden. Sie sind also in der Freiheit eingeschränkt und haben keinen Einfluss auf die Qualität der Daten.
Auch ein Vorher-Nachher-Vergleich ist grundsätzlich zulässig. In diesem Fall erheben Sie Daten von denselben Personen zu unterschiedlichen Zeitpunkten – z.B. einmal vor Anwendung der DiGA unter herkömmlicher Behandlung und einmal nach Anwendung der DiGA. Doch auch hier muss die Behandlung zum ersten Messzeitpunkt der Versorgungsrealität entsprechen. Dieses Vorgehen ist hauptsächlich bei stabilen Zuständen sinnvoll, in denen eine herkömmliche Behandlung keine Verbesserung mehr erzielt (z.B. Diabetes).
3.3 Endpunkte
Die Endpunkte einer Studie beschreiben ihre angestrebten Ziele. Grundsätzlich können Sie beliebig viele Endpunkte definieren, der primäre Endpunkt wird aber der angestrebte positive Versorgungseffekt sein – z.B. Verbesserung der Lebensqualität. Die Nutzenbewertung kann über beliebig viele Endpunkte gemessen werden.
Je mehr Endpunkte Sie untersuchen und je mehr Nutzennachweise Sie erbringen können, desto vorteilhafter ist dies für die Preisverhandlungen. Bei der Definition von Endpunkten helfen Erkenntnisse aus der Literatur und der Pilotstudie (falls eine solche vorliegt). Je mehr primäre Endpunkte Sie definieren, desto teurer wird aber auch die Studie z. B. aufgrund einer größeren Stichprobengröße. Die meisten erfolgreichen DiGA beschränken sich auf genau einen primären Endpunkt.
Für die reine Aufnahme ins DiGA‑Verzeichnis ist der Nutzennachweis für einen patientenrelevanten Endpunkt ausreichend. Auch wenn sie nicht komplett deckungsgleich sein müssen, müssen Endpunkte konsistent mit der Zweckbestimmung der Anwendung sein.
Wichtig: Es zählen nur patientenrelevante Endpunkte. Endpunkte, die keinen Nutzen für den Patienten darstellen, spielen beim BfArM keine Rolle. Dazu zählen beispielsweise ökonomische Aspekte.
3.4 Hypothesen
Jede Studie muss konkrete Hypothesen untersuchen. Diese müssen so formuliert sein, dass sie entweder beleg- oder auch widerlegbar sind. Bei Hypothesen handelt es sich um klare Aussagen, die überprüft werden sollen. Idealerweise formulieren Sie für jeden Endpunkt, für den Sie einen Effekt nachweisen wollen, eine eigene Hypothese.
Beispiele:
- Patienten, die die DiGA verwenden, haben nach sechs Monaten eine höhere Lebensqualität als Patienten, die eine herkömmliche Behandlung erhalten.
- Unter Einsatz der DiGA verkürzt sich die Behandlungsdauer im Vergleich zu einer herkömmlichen Therapie.
3.5 Methode
Bei der Messung von Endpunkten müssen anerkannte Methoden eingesetzt werden. Zudem sind Endpunkte auch oft nur durch Selbstauskünfte der Studienteilnehmer messbar. Zum Beispiel gibt es kein Maßband, welches die Lebensqualität eines Menschen punktgenau messen kann. Die wichtigsten Methoden sind medizinische Messgeräte und psychologische Fragebögen.
Beispiele für Messinstrumente für einige positive Versorgungseffekte:
- Lebensqualität:
- SF-36/SF-12
- SWLS – Satisfaction with Life Scale
- EuroQoL (EQ)-5D
- Bewältigung der Schwierigkeiten im Alltag:
- SASS – Soziale Aktivität Selbstbeurteilungs-Skala
- GAF – Global Assessment of Functioning
- Patientensouveränität/Selbstwirksamkeit:
- ASKU – Allgemeine Selbstwirksamkeitserwartung
- SWOP-9 – Fragebogen zu Selbstwirksamkeit-Optimismus-Pessimismus
Wenn Sie eigene Messmethoden einsetzen, müssen diese erst validiert werden.
3.6 Minimal Clinically Important Difference (MCID)
Der Minimal Clinically Important Difference (MCID) beschreibt den kleinstmöglichen Unterschied in einem Endpunkt, der für Patienten tatsächlich eine spürbare und relevante Verbesserung darstellt. Er hilft dabei einzuschätzen, ob ein statistisch signifikanter Effekt auch klinisch bedeutsam ist. In der Praxis führt genau dieser Punkt häufig zu Diskussionen zwischen Herstellern und dem BfArM: Während Hersteller einen bestimmten Effekt als ausreichend relevant ansehen, kann das BfArM diesen als klinisch nicht bedeutsam einstufen. Die Definition eines angemessenen MCID ist daher ein zentraler Bestandteil der Studienplanung und sollte frühzeitig gut begründet werden.
4. Evaluationskonzept (bei vorläufiger Aufnahme)
Bei einer vorläufigen Aufnahme möchte das BfArM natürlich zumindest einen Anhaltspunkt dafür, warum Ihre DiGA einen positiven Versorgungseffekt erzielen kann und wie man plant, diesen nachzuweisen.
Dies wird in Form eines Evaluationskonzepts sichergestellt und hier gilt eine sorgfältige Herangehensweise. Das Konzept muss von einer herstellerunabhängigen Institution erstellt werden und den allgemeinen wissenschaftlichen Standards entsprechen. Wichtig ist, dass das Evaluationskonzept zum Nachweis des positiven Versorgungseffekts geeignet ist, denn sie müssen sich bei der Durchführung der Studie auch an dieses Konzept halten.
Ein guter Grundstein für das Evaluationskonzept ist die verpflichtende “systematische Nutzerdatenauswertung”. Diese erfolgt auf Basis von Daten, die mit der DiGA erhoben wurden. Auch wenn es nicht öffentlich vom BfArM erwähnt wird, ist darunter eine Pilotstudie zu verstehen.
Diese sollte nicht unterschätzt werden! Das bedeutet nämlich unter anderem, dass Sie ein Ethikvotum dafür brauchen. Dafür ist von einer Wartezeit von mehreren Wochen oder gar Monaten auszugehen. Auch bei der Nutzerdatenauswertung muss Ihre Stichprobe eine gewisse Größe erreichen, um eine gewisse Aussagekraft zu haben (z.B. 50 Personen).
Des weiteren ist eine Literaturrecherche ist für das Evaluationskonzept notwendig. Diese soll einen Überblick über den aktuellen Stand der Forschung in Ihrem Bereich geben und Anhaltspunkte dafür liefern, welche Endpunkte untersucht werden. Die Ergebnisse der Nutzerdatenauswertung sollen zeigen, dass die DiGA funktioniert und den angestrebten Effekt bewirken kann.
Untersuchen Sie in Ihrer Pilotstudie gerne mehrere Endpunkte. Dies hilft Ihnen bei der späteren Fallzahlplanung und Sie können dann entscheiden, welche Endpunkte Sie auch in der geplanten Studie untersuchen möchten.
Dem Evaluationskonzept sind auch noch weitere Dokumente beizulegen. Ein Dokument, auf welches das BfArM ein besonderes Auge wirft, ist das Studienprotokoll. Hier sind insbesondere logistische Aspekte der Studie definiert, wie beispielsweise die Finanzierung, das Datenmanagement und Verantwortlichkeiten. Manche Informationen doppeln sich im Evaluationskonzept und dem Studienprotokoll. Achten Sie darauf, dass auch im Studienprotokoll alle relevanten Informationen enthalten sind.
Auch ein statistischer Analyseplan ist obligatorisch. Dieser enthält unter anderem Informationen zu Randomisierung, Verblindung, Endpunkten, Umgang mit fehlenden Daten und statistischer Analyse.
QuickBird Medical Tipp: Vor Durchführung der Pilotstudie empfehlen wir einen Termin beim BfArM, um die Studiensynopse zu besprechen.
4.1 Fristen in der Erprobungsphase
Mit dem Bescheid über die vorläufige Aufnahme ins DiGA-Verzeichnis gibt es kaum eine Verschnaufpause. Denn dann starten die 12 Monate, in denen DiGA-Hersteller die Möglichkeit haben, die geforderten Studienergebnisse vorzulegen. In diesem Zeitraum muss die Studie gemäß dem Evaluationskonzept vollständig durchgeführt und ausgewertet werden.
Gesetzlich ist zwar ein Antrag auf die Verlängerung des Erprobungszeitraums möglich, dieser muss aber plausibel begründet werden und ist beim BfArM ungern gesehen. Grundsätzlich gilt: kann der Nachweis aus eigenem Verschulden heraus nicht erbracht werden (z. B. durch falsche Planung), wird der Antrag abgelehnt. Zulässig sind nur externe Faktoren, wie etwa die Corona-Pandemie, wodurch die Studie nicht nach Plan durchgeführt werden konnte.
Spekulieren Sie also nicht schon zu Beginn auf die Verlängerung dieses Zeitraums. Wenn dies dem BfArM auffällt, wird auch der Antrag auf Erprobung abgelehnt.
Eine Verlängerung muss spätestens drei Monate nach Ablauf der Frist beantragt werden. Sie sollten allerdings sofort mit dem BfArM Kontakt aufnehmen, sobald sich abzeichnet, dass Sie diese nicht einhalten können.
5. Zusammenfassung
Der Nachweis eines positiven Versorgungseffekts ist essenziell für die dauerhafte Listung im DiGA-Verzeichnis. Der positive Versorgungseffekt wird in zwei Kategorien unterteilt: medizinischer Nutzen und patientenrelevante Struktur- und Verfahrensverbesserung.
Der positive Versorgungseffekt muss im Antrag gemeinsam mit der Patientengruppe (ICD-Code) spezifiziert werden. Den angegebenen Nutzen muss jeder Hersteller für seine DiGA im Zuge einer empirischen Studie nachweisen. Das BfArM hat hohe Anforderungen an derartige Studien. So gilt beispielsweise als Mindestanforderung, dass es sich um eine vergleichende Studie handeln muss. Empfehlenswert sind hierbei insbesondere randomisierte kontrollierte Studien.
Anforderungen an die Studie im Überblick:
- Es muss mindestens eine vergleichende Studie sein
- Die DiGA muss mit der Versorgungsrealität verglichen werden
- Die Studie muss einen positiven Unterschied in einem patientenrelevanten Endpunkt nachweisen
- Zur Messung von Endpunkten müssen validierte Messinstrumente eingesetzt werden
- Der Durchführungsort der Studie muss Deutschland sein
- Die Studie muss in einem öffentlichen Register eingetragen werden
- Die Studienergebnisse müssen vollständig veröffentlicht werden
Anträgen zur vorläufigen Aufnahme ins DiGA-Verzeichnis ist ein Evaluationskonzept beizulegen, welches zumindest belegt, dass die DiGA funktioniert und es Anhaltspunkte für positive Versorgungseffekte gibt.
Inhalte des Evaluationskonzepts (bei vorläufiger Aufnahme):
- Genaues Vorgehen bei der Studie
- Systematische Nutzerdatenauswertung (Pilotstudie)
- Literaturrecherche
- Studienprotokoll
- Statistischer Analyseplan
QuickBird Medical übernimmt die Entwicklung und Regulatorik Ihrer DiGA und begleitet Sie bis zur Aufnahme ins BfArM-Verzeichnis. Kontaktieren Sie uns jederzeit, falls Sie Fragen haben, oder ein konkretes Projekt umsetzen möchten.





